抱歉,我們並不支援你正使用的瀏覽器。
為達至最佳瀏覽效果,請更新至最新的瀏覽器版本。
如有問題,歡迎電郵至 pccwmediaiapps@pccw.com 查詢。
為達至最佳瀏覽效果,請更新至最新的瀏覽器版本。
如有問題,歡迎電郵至 pccwmediaiapps@pccw.com 查詢。
廣告
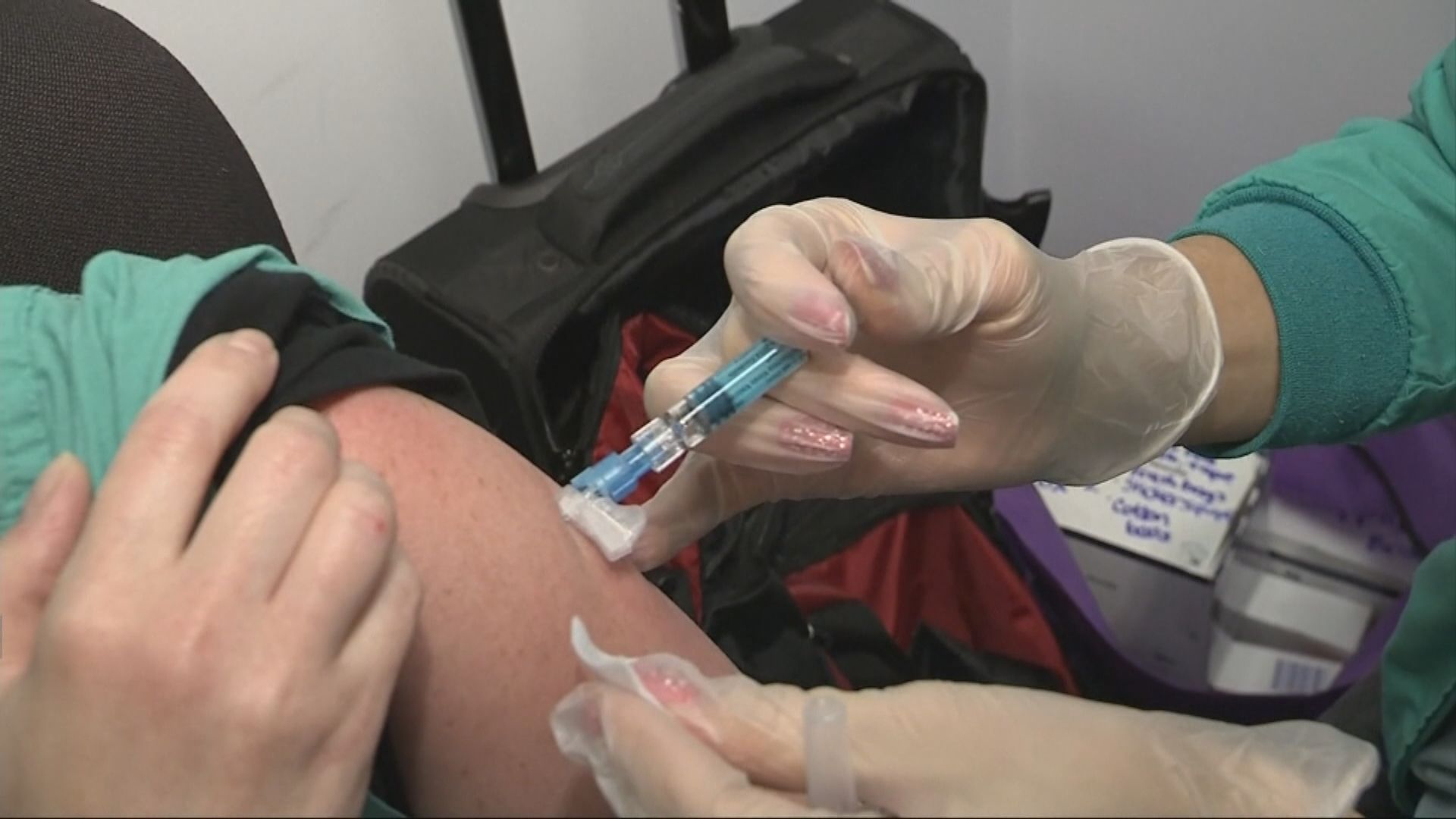
【Now新聞台】美國食品及藥物管理局局長哈恩表示,願意在對公共衞生帶來好處的前提下,考慮在疫苗完成第三期臨床試驗前,緊急授權使用疫苗,他強調此舉並非要討好總統特朗普。
新型冠狀病毒仍然肆虐,疫苗何時能面世並投入使用,是全球關注焦點。
繼中國及俄羅斯批准緊急使用新冠疫苗後,美國食品及藥物管理局局長哈恩接受《金融時報》訪問時表示,願意考慮繞過正常審批程序,在疫苗完成第三期臨床試驗前緊急授權使用,但前提是這樣做,對突發公共衞生事件的好處大過風險。
哈恩表示,是否申請緊急授權使用,由研發疫苗的機構決定,如果他們於三期臨床試驗結束前提交申請,食品及藥物管理局會對此作出裁決,哈恩強調即使批准,只會緊急授權用於特定群組,而非全面批准。
美國總統特朗普早前曾表示,對疫苗可在11月大選前面世感到樂觀,令不少醫生憂慮,特朗普會為此向食品及藥物管理局施壓。
哈恩就說,緊急授權使用疫苗是基於科學、醫學和數據,與政治原因無關,不會為了討好特朗普而倉卒批准申請。
不過藥管局前局長戈特利布就認為應該待完成試驗,才可以評估疫苗的成效,又指相信要等到11月,才有第三階段的疫苗試驗數據。
美國生物科技公司莫德納及藥廠輝瑞分別研發的疫苗,已在美國進入第三階段臨床測試,各招募三萬人進行試驗,每人需要打兩針。
另外兩間公司阿斯利康和諾瓦瓦克斯分別研發的疫苗,同樣需要打兩針,疫苗正式面世後,民眾可能要接種兩劑,才能確保有效。


